급성기 척수손상 환자의 하루 시간대별 심박변이도 변화 : 손상 수준에 따른 자율신경계 반응 비교
© 2026 by the Korean Physical Therapy Science
Abstract
Although heart rate variability(HRV) has been studied in individuals with spinal cord injury(SCI), most investigations have emphasized chronic stages or focused on nocturnal measurements, leaving daytime HRV dynamics in acute SCI largely unexplored. The objective of this study was to characterize diurnal HRV patterns in the acute stage of SCI and to evaluate differences in autonomic regulation between patients with injuries at or above T6 and those with injuries below T6.
Repeated measures observational study.
This repeated measures observational study evaluated HRV at six time points throughout a single day at 2-hour intervals (from 8AM to 6PM). A total of 60 patients with acute SCI(30 with injuries at or above T6 and 30 with injuries below T6), admitted to 3 rehabilitation hospitals between 2020 and 2024, were included. HRV parameters—including standard deviation of NN intervals(SDNN), root mean square of successive differences(RMSSD), high-frequency(HF), low-frequency(LF), very low frequency(VLF), and the LF/HF ratio—were recorded using the SA-3000NEW device. Repeated-measures analysis of variance(ANOVA) was conducted to assess temporal changes, adjusting for age and sex as covariates.
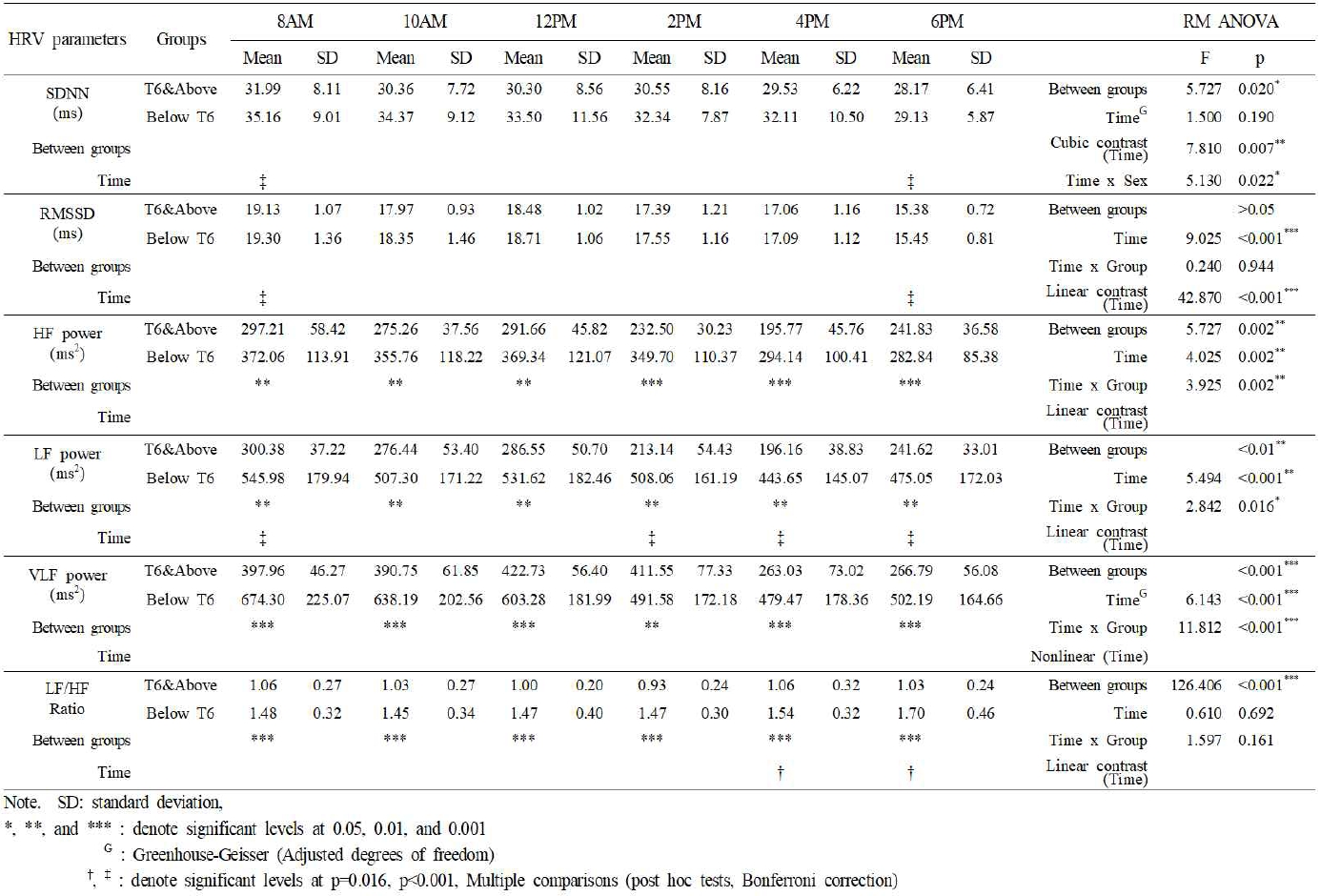
Group differences were significant in SDNN, HF, LF, and VLF, with the Below T6 group consistently showing higher values across all time points. RMSSD showed a significant time effect, but no group difference. LF/HF ratio showed a significant main group effect without a time effect. Notably, certain time-of-day differences, particularly between 08:00 and 18:00, were statistically significant.
HRV in acute SCI patients demonstrated distinct temporal patterns and significant differences based on injury level. Patients with injuries below T6 exhibited more stable autonomic function throughout the day. These results highlight the need to account for both circadian timing and lesion level when assessing autonomic dysfunction during early rehabilitation.
Keywords:
autonomic nervous system, spinal cord injury, heart rate variability, heart rateⅠ. 서 론
척수손상(spinal cord injury, SCI), 특히 상위 경수 신경 손상 환자에서는 교감신경계 기능 저하로 인한 저혈압, 심장부정맥, 기립성 저혈압, 자율신경 반사이상(autonomic dysreflexia) 등 다양한 심혈관계 합병증이 흔하게 발생한다(West 등, 2013; Myers 등, 2007). SCI가 심혈관계 기능에 미치는 영향을 다룬 여러 연구를 통해 밀접한 연관성이 밝혀졌으나, 손상 정도가 각기 다른 환자들의 개별적인 생리학적 반응에는 이질성이 존재하며, 척수신경의 손상부위와 정도에 따른 자율신경계 반응성 및 이에 영향을 미치는 재활 중재에 대한 연구는 여전히 부족하다(Schoffl 등, 2024; Hodgkiss 등, 2023).
최근에는 SCI 환자의 심장 자율신경 기능을 정량적으로 평가하기 위한 방법으로 심박변이도(heart rate variability, HRV)가 광범위하게 활용되고 있다. HRV는 심장 박동 간 시간 간격의 변동성을 의미하며, 이는 심혈관계가 외부 자극이나 스트레스에 얼마나 효과적으로 반응하고 회복하는지를 반영하는 지표이다(Yadav 등, 2025; Addleman 등, 2024; Park 등, 2024; Ruangsuphaphichat 등, 2023; Schoffl 등, 2023; Solinsky 등, 2021). 교감신경계는 주간에 더 활성화되어 심박수가 증가하고 HRV는 감소하는 반면, 부교감신경계는 야간에 더 우세해져 심박수가 감소하고 HRV는 증가하는 경향을 보인다(Zhang 등, 2025; Ma 등, 2023). 이처럼 HRV는 일주기적(circadian) 변동 양상을 가지며, 야간에 높아지고, 주간에는 낮아지는 패턴이 주로 관찰된다. 특히 HRV의 고주파(HF) 성분은 주로 부교감신경 활성과 연관되며 야간에 증가하고, 저주파(LF) 성분은 교감 및 부교감 신경 모두 관련되며 주간에 증가한다(Deshpande 등, 2016; Taralov 등, 2015; Morris 등, 2012). 하지만 SCI 환자에게는 정상인과 상대적으로 다른 양상을 보인다. 선행연구에 따르면, 경수 손상 환자에서는 LF 파워의 감소, 흉수 손상 환자에서는 HF 파워의 감소가 주로 관찰되었다(Calderon-Juarez 등, 2024; Park 등, 2024; Stampas 등, 2023; de Carvalho Abreu, Dias 등, 2016).
자세 변화에 따른 HRV 반응을 비교한 연구에서는 건강한 성인은 교감-부교감 활성의 조절 변화가 뚜렷하게 나타나지만, SCI 환자에서는 이러한 변화가 거의 관찰되지 않았다(de Carvalho Abreu 등, 2016). 척수손상 부위가 흉-요수 신경에서 경수손상의 부위로 올라갈수록 심혈관계 조절 기능이 더 크게 손상되었고, 교감신경계의 활성도 감소와 연관성이 있음을 보여준다. 이렇게 현재까지 SCI 환자를 대상으로 24시간 동안 HRV를 평가한 연구는 일부 존재하나(Saengsuwan 등, 2024; Malmqvist 등, 2015), 대부분 퇴원 후 일상생활을 수행하고 있는 비교적 안정된 상태의 환자를 대상으로 하였고(Saengsuwan 등, 2024; De Maria 등, 2023; Rosado-Rivera 등, 2011), SCI 발생 초기의 입원환자 대상 연구도 보고되었으나, 1회성이거나 하루 2번(아침, 저녁) 혹은 입원 기간 중 3회(입원, 중간, 퇴원) 평가하였고(Stampas 등, 2023; Buker, 등, 2018; Malmqvist 등, 2015), 일상 생활 속에서의 척수손상 레벨에 따른 HRV 변화 양상을 살펴본 연구는 부족하다.
본 연구는 SCI 초기 입원 환자를 척수신경 손상 T6를 기준으로 구분하여, 발병 초기 입원 SCI 환자의 낮 시간대의 HRV 파라미터들의 변화 패턴을 파악하고, 자율신경계 기능의 차이를 분석하여, 향후 여러 재활 중재의 효과를 비교하기 위한 기초 자료를 마련하고자 한다.
Ⅱ. 연구방법
1. 연구대상
본 연구는 반복측정 연구관찰(Repeated measures observational study)로서 2020년 5월 2일부터 2024년 12월 28일까지 K병원, R병원, S병원에 입원한 발병 6개월 이내 SCI 환자를 대상으로 실시하였다. 연구 대상은 SCI 진단을 받은 환자 중, 흉수 6번(T6) 손상 수준을 기준으로 상위 손상군(T6 & Above)과 하위 손상군(Below T6)으로 구분하였다(Saengsuwan 등, 2024: Serra-Ano 등, 2015).
포함기준은 입원환자 중 집중 재활치료를 위하여 재활의학과로 전과된 초기 SCI 환자 중에서 휠체어 이동이 가능한 환자, 만 18세 이상을 대상으로 하였다. 제외 기준은 중증 경직, 뇌손상, 기계적 인공호흡, 산소치료, 비정상적인 호흡 패턴(호흡 속도 분당 20회 이상 또는 분당 10회 미만), 발열(체온≥37.4°C), 동반되는 심장 질환 및 당뇨병과 갑상선 질환을 포함한 내분비 장애는 제외하였고, 양극성 장애 또는 정신병 진단력이 없는 경우이며, 카페인 섭취 및 자율신경계 반사부전 증상은 제외하였다(Ruangsuphaphichat 등, 2023; Tsou 등, 2022).
반복측정 ANOVA를 위한 표본 크기 산출에는 G*Power 3.1.9.4를 사용하였고, 중간 정도(f = 0.25)의 효과 크기를 적용(Effect size f=0.25, α=0.05, 2그룹 각 6회 측정, 산출된 샘플크기 76명) 하였다(Henry 등, 2024; Zimmermann 등, 2019; Kim, 2016). 중간에 누락되는 인원을 고려하여 약 4년 동안 K병원, R병원, S병원에 입원하는 SCI 환자를 대상으로 하였다. 모든 참가자는 연구 참여 전 서면 동의서를 작성하였다. 입원 중 재활 프로그램의 영향을 최소화하기 위해 평일이 아닌 일요일에 HRV를 측정하였고, 검사 당일 최대한의 안정 상태에서 진행하였다(김현철 등, 2020).
2. 측정도구와 자료 수집과정
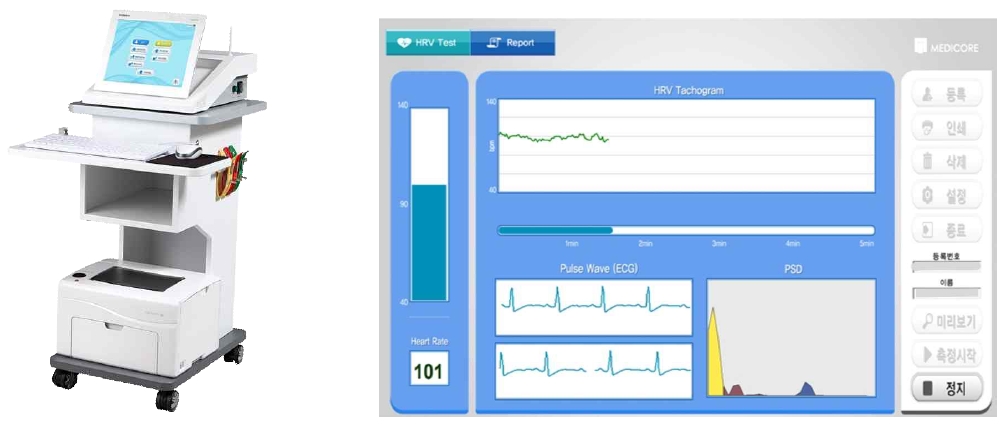
모든 참가자는 먼저 인구학적 및 임상적 특성에 대한 설문지를 작성한 후, MEDICORE HRV Analyzer SA-3000NEW(Figure 2)를 사용하여 심박변이도를 측정하였다(임창하 등, 2024; Tsou 등, 2022). 참가자들은 조용하고 밝은 실내(온도 20~25°C)에서 심리적인 안정을 취하기 위해 1명의 보호자만 들어올 수 있도록 입실을 제한하였다. 측정 당일 카페인 섭취를 금지하고, 검사 24시간 전부터 알코올을 마시지 않도록 하였고, 자극성 음식 및 음료 섭취를 제한하고, 금속류 착용을 금하였다(Flueck 등, 2016).
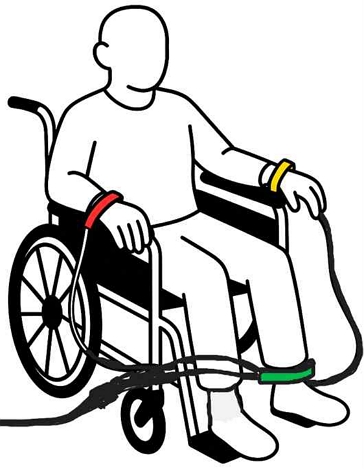
측정 자세는 의자 또는 휠체어에 등받이를 댄 상태로 앉아 눈을 감지 않도록 안내하였으며, 측정 중에는 움직이거나 말하지 않고 정상적으로 호흡하도록 요청하였다(Chuangchai 등, 2021). 3가지 전극 중, 붉은 전극은 오른쪽 손목에 부착하고, 노란색 전극은 왼쪽 손목에 부착, 녹색 전극은 왼쪽 발목에 부착하였다(Figure 3).
측정 전 10분간 안정을 취한 후에 5분간 자연 호흡을 유지하며 HRV를 검사하였다. T6 & Above 그룹 환자의 특성상, 식사시 보호자 도움이 필요하고, 휴식시간, 약물복용, 체위변경, 방광관리(넬라톤, 자가도뇨) 등의 환경적인 요인으로 인해 급성기 입원환자에게 2시간 간격으로 측정하였다.
HRV 측정은 오전 8시부터 2시간 간격으로 오후 6시까지 총 6회 진행되었고, 측정시간 외에는 편안하게 일상 생활 및 휴식을 취하였다. 가급적 측정 기준시간의 ±5분 이내의 오차범위에서 시작하였고, 만약 오전 8시5분에 측정을 시작한 참가자가 있다면, 그 이후 평가도 모든 해당 시각의 5분에 측정을 시작하였다(Figure 2. A, B).
HRV는 교감 및 부교감신경의 활성 상태를 정량적으로 평가할 수 있는 지표이며, 시간 영역(SDNN, RMSSD 등)과 주파수 영역(LF, HF, VLF, LF/HF 등)으로 나누어 자율신경계의 기능을 정량화 할 수 있다(van Es 등, 2024; Park 등, 2022; Tsou 등, 2022; Kim 등, 2021; 김현철 등, 2020). 시간 영역 지표는 평균 심박수(Heart Rate, HR) 외에 기록시간 동안의 심장 박동의 R-R interval 변화 정도를 통계 처리한 값인 정상 간격의 표준편차 (SDNN)와 연속한 정상 박동 간의 차이의 제곱평균근(RMSSD)이다. 주파수 영역 지표는 R-R interval의 변화를 각 주파수 대역별 파형으로 분리하여 극저주파(Very Low Frequency, VLF), 저주파(Low Frequency, LF), 고주파(High Frequency, HF) 영역에서 측정되었다(Table 1).
HF 파워는 0.15~0.40Hz의 주파수 범위 내에 있는 HRV의 스펙트럼 성분으로, 주로 부교감신경(미주신경) 활동의 영향을 받으며 호흡 부비동 부정맥과 밀접한 관련이 있다(Nagai 등, 2025; Kiyono 등, 2017). HF 파워는 ms² 단위로 측정한 HF 성분의 크기이며, 부교감 신경계 기능의 신뢰할 수 있는 지표이다(Kuzmenko 등, 2022; Deshpande 등, 2016). 심부 고주파 파워의 감소는 미주신경 긴장도 감소와 관련이 있으며, 이는 심부전, 당뇨병, 불안 장애와 같은 질환에서 흔히 관찰된다(Nagai 등, 2025; Kiyono 등, 2017). HF 파워는 호흡 패턴에 크게 영향을 받기 때문에 호흡기와 관련된 부교감신경 활동을 평가하는 데 유용한 도구이다(Kuzmenko 등, 2022; Graff 등, 2013). 허혈성 뇌졸중 환자에서 HF 출력이 높을수록 기능적 결과가 향상되어 회복과 예후에 미치는 역할이 강조된다(Graff 등, 2013).
LF 파워는 0.04~0.15Hz의 주파수 범위 내에서 HRV의 스펙트럼 성분이다. 교감신경과 부교감신경 활동의 영향을 모두 받지만 교감신경 조절과 더 밀접하게 연관되어 있다(Kiyono 등, 2017). LF 파워는 ms² 단위로 측정한 LF 성분의 크기이며, 심박수에 대한 교감신경 영향의 강도를 반영한다(Cowan, 1995). LF 파워 상승은 종종 교감신경계 활동 증가를 나타내는 지표로 해석된다. 이는 고혈압, 심부전, 스트레스 관련 장애 등의 질환에서 흔히 관찰된다(Kiyono 등, 2017). 손상 수준이 낮을수록(Below T6) 높게 측정되며, 이는 남아있는 교감신경 및 부교감신경 조절력과 관련이 있다(Saengsuwan 등, 2024).
LF/HF 비율은 LF 파워를 HF 파워로 나누어 계산하고, 교감신경과 부교감신경 활동의 균형을 나타내는 지표로 자주 사용된다(Kuzmenko 등, 2022). LF/HF 비율이 높을수록 교감신경이 우세하다는 것을 나타내며, 낮은 비율은 부교감신경이 우세함을 나타낸다. 이 비율은 고혈압, 심부전 및 신경계 장애와 같은 질환의 자율 신경 기능 장애를 평가하는 데 유용하다(Kiyono 등, 2017; Oka, 2017).
모든 HRV 지표는 SA-3000NEW 분석기를 통해 추출된 후, SPSS 30(IBM Corp., USA)을 사용하여 분석하였다. 연속형 변수는 평균±표준편차(Mean±SD)로, 범주형 변수는 빈도(n)와 백분율(%)로 제시하였다. 데이터의 정규성 검증은 Shapiro-Wilk 검증을 하였고, 임상적 특성 및 각 변수별 초기값의 비교는 정규성 만족시 t-test, 정규성 불만족시 Mann-Whitney U 검정을 하였다. 그룹 간 및 그룹 내 변수 비교는 T6 & Above 그룹과 Below T6 그룹을 대상으로 6회 측정 값에 대한 반복측정 분산분석(repeated measures of ANOVA)을 수행하였다. 통계적 유의수준은 양측 기준으로 P<0.05로 설정하였다. 단일 시간대별, 그룹 간 차이 검정이 필요한 경우에는 독립표본 T검정 및 Mann-Whitney U 검정을 추가로 시행하였다. 심박변이도 분석시 성별 및 나이를 따로 고려할 필요가 있다는 이전 연구에 따라, 성별(더미 변환), 나이 변수를 공변량으로 선택하였다(De Maria 등, 2023; 신숙희 등, 2014).
Ⅲ. 연구결과
1. 연구 대상자의 일반적 특성
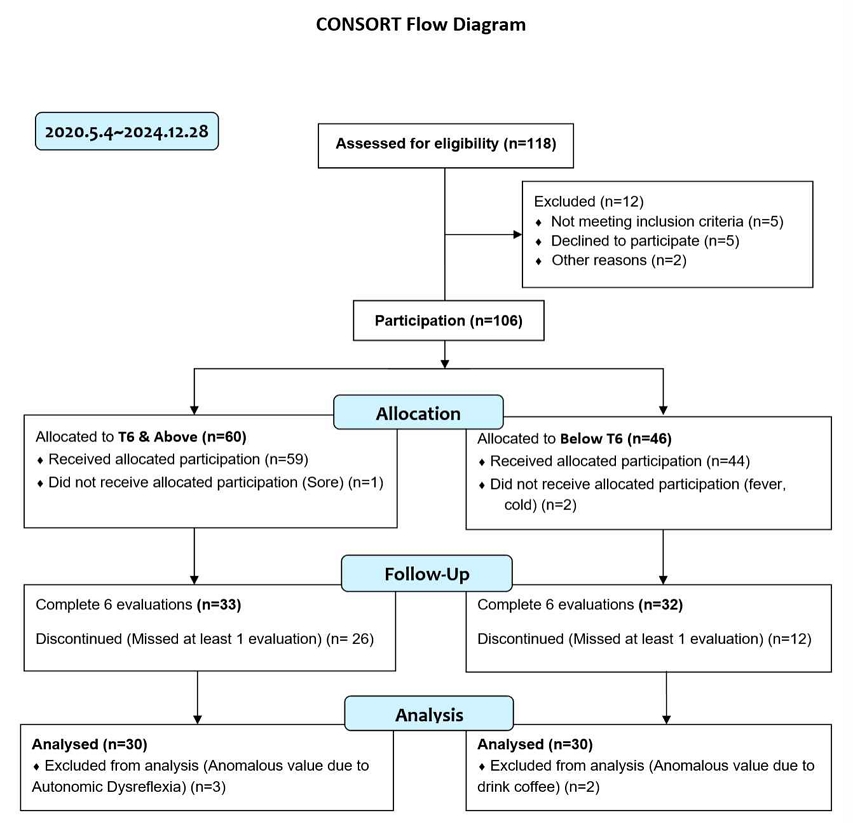
본 연구에는 4년 8개월 동안 총 118명의 SCI 환자를 모집하였고, 설명을 듣고 참여를 거절하거나 조건에 해당하지 않는 12명을 제외한 106명을 T6 레벨 기준으로 위/아래로 구분하였다. 평가일에 욕창, 발열, 감기 증상을 보인 3명 제외, 6회 평가 중 1회 이상 측정하지 못한 T6 & Above -26명, Below T6 -12명이 누락되어, 최종 65명이 6회 측정 완료하였다(Figure 3). 그러나 두 그룹에서 평균으로부터 3표준편차 이상 벗어난 이상치로 확인된 5명(T6 & Above -3명, Below T6 -2명)은 추가 탈락되었다. 사유는 자율신경계 반사부전증 3명과 점심시간에 몰래 커피를 복용한 경우였다. 모집된 T6 & Above 그룹은 60명, Below T6 그룹은 46명이다. 측정을 진행하면서 컨디션 저하 및 긴급 퇴원 등 중간 탈락자가 발생하였고(T6 & Above -2명, Below T6 -16명), 6회 측정 완료된 최종 인원은 각 30명씩이었다. 두 군 간 연령, 키, 몸무게, BMI는 통계적으로 유의한 차이가 없었다(Table 2). 교육 수준은 두 군 모두 고등학교 이상 학력이 대다수를 차지하였다.
동반 질환은 T6 & Above 그룹에서 30.0%가 1개 이상의 질환(천식 20%, 폐렴 16.7%, 당뇨 23.3%, 고혈압 53.3%, 고지혈증 40.0%)을 가지고 있었으며, Below T6 그룹에서는 26.7%의 동반질환(천식 23.3%, 폐렴 16.7%, 당뇨 13.3%, 고혈압 46.7%, 고지혈증 33.3%)이 확인되었다. 약물 복용 여부는 T6 & Above 그룹의 60.0%에서 고혈압약 등 1개 이상의 약물을 복용 중이었고, Below T6 군에서는 55.5%가 약물을 복용 중이었다. 손상의 주요 원인은 교통사고가 51.7%로 가장 많았으며, 손상 부위는 경수 45.0%, 흉수 21.7%, 요수 33.3%의 순으로 나타났다. 하지마비 환자는 주로 흉수 손상(46.3%)과 연관되었고, 사지마비 환자는 경수 손상(81.8%)과 관련되었다. 척수 손상 정도는 완전 하지마비 2명, 불완전 하지마비 5명, 완전 사지마비 1명, 불완전 사지마비 52명으로 분포하였다.
2. 시간영역 지표(Time domain parameters)
Standard deviation of all normal-to-normal R-R interval(SDNN)
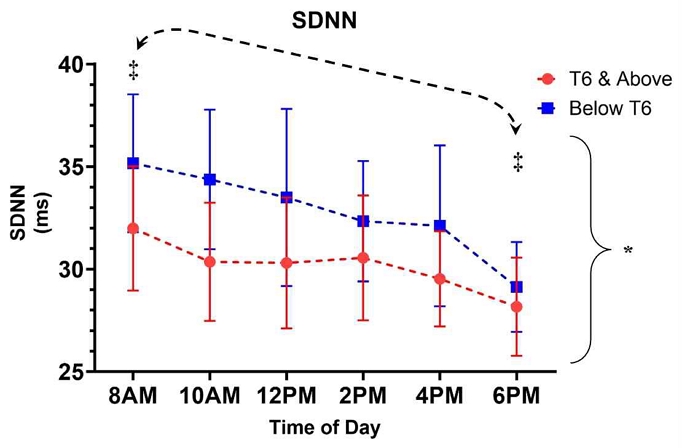
SDNN 지표의 경우, 구형성 가정이 충족되었고(Mauchly’s W 0.743, p=0.309), 그룹 간 주효과는 유의하게 나타났고, T6 & Above 그룹과 Below T6 그룹 간의 평균에 유의한 차이가 있었다(F(1,56)=5.727, p=0.020, η²ₚ=0.093). 시간의 주효과는 유의하지 않았으며(F(5,280)=1.500, p=0.190, η²ₚ=0.026), 시간과 그룹 간 상호작용도 통계적으로 유의하지 않았다(F(5,280)=0.283, p=0.922, η²ₚ=0.005). 그러나 삼차 대비에서는 시간의 변화가 유의한 차이를 보였으며(F(1, 56)=7.81, p=0.007, η²=0.122), 이는 하루 중 특정 시간대에서의 변화가 급격하다는 가능성을 시사한다. 사후검정(Bonferroni 조정)에 따르면, 8AM과 6PM 사이에서만 통계적으로 유의한 차이(p=0.011)가 관찰되었다. 다른 시간대에서도 그룹 간 평균 차이는 관찰되지만, 분산 차이와 표준편차의 영향으로 통계적 유의성은 나타나지 않았다. 모든 시간대에서 Below T6 그룹의 평균 SDNN이 일관되게 더 높게 나타났으며, 특히 오전 10시에서 가장 큰 차이(+4.01ms)를 보였다. 또한 시간과 성별 간의 유의한 3차 대조 상호작용을 제외하고는 유의한 성별 효과나 시간×성별 상호작용은 발견되지 않았다(F(1, 57)=5.13, p=0.021, η²ₚ=0.091)(Figure 4).
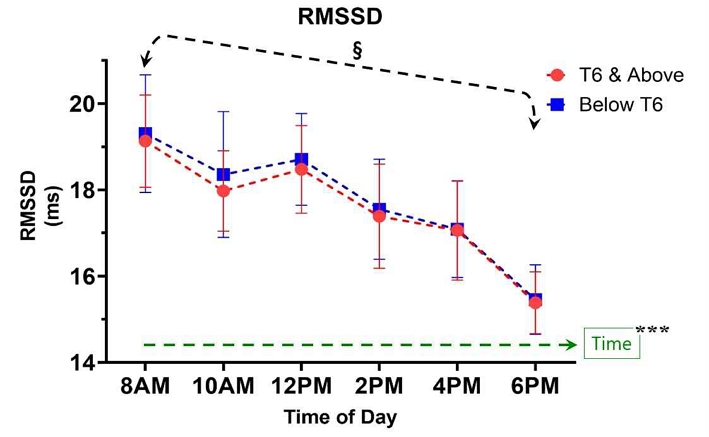
Root-mean-square of successive differences(RMSSD)
RMSSD 지표의 경우, 구형성 가정이 충족되지 않았고(Mauchly’s W=0.558, p=0.005), 시간에 따라 통계적으로 유의한 변화를 보였다(F(5, 280)=9.025, p<0.001, η²=0.139). 그러나, 시간과 손상레벨(그룹) 간에 상호작용 효과는 유의하지 않았다 (F(5, 280)=0.24, p=0.944, η²=0.004). 각 시간대에서 그룹 간의 RMSSD 차이를 검정한 결과, 모든 시간대에서 그룹 간 차이는 통계적으로 유의하지 않았다(모든 p>0.05). RMSSD의 시간 경과에 따른 변화는 확인되었으나, 손상 레벨의 영향은 제한적인 것으로 해석될 수 있다. 시간에 따른 RMSSD의 변화(주효과)는 Greenhouse-Geisser 수정 자유도를 기준으로 유의하였다(F(4.13, 231.34)=9.025, p<0.001, η²=0.139). 집단(Group), 성별(Sex), 나이(Age)와 시간 간의 상호작용 효과는 모두 통계적으로 유의하지 않았다(모든 p>0.3). 다중비교 (Bonferroni 조정)에 따르면, 오전 8시와 오후 6시 사이의 평균 RMSSD는 유의미하게 감소하였다(p<0.001). 10AM과 12PM 사이 및 2PM과 4PM 사이를 제외한, 모든 인접 시간대에서 유의미한 감소 경향 확인되었다. 단일 시간대별 그룹 간 차이를 확인하기 위한 독립표본 T검정 및 Mann-Whitney U 검정 결과, 모든 시간대에서 T6 이상 그룹과 Low T6 그룹 간 유의미한 차이는 나타나지 않았고(p>0.05), 그룹별 RMSSD 변화는 유사한 추세를 보였으며, 명확한 상호작용은 없었다. 선형 대비 결과에서는 시간에 따른 RMSSD의 점진적인 감소가 통계적으로 유의하였다(F(1, 56)=42.870, p<0.001, 부분 η²=0.4371). Levene의 등분산성 검정과 Box의 M 검정 모두 유의하지 않아 공분산 행렬의 동질성 가정을 만족하였다(Figure 5).
3. 주파수 영역 지표(Frequency domain parameters)
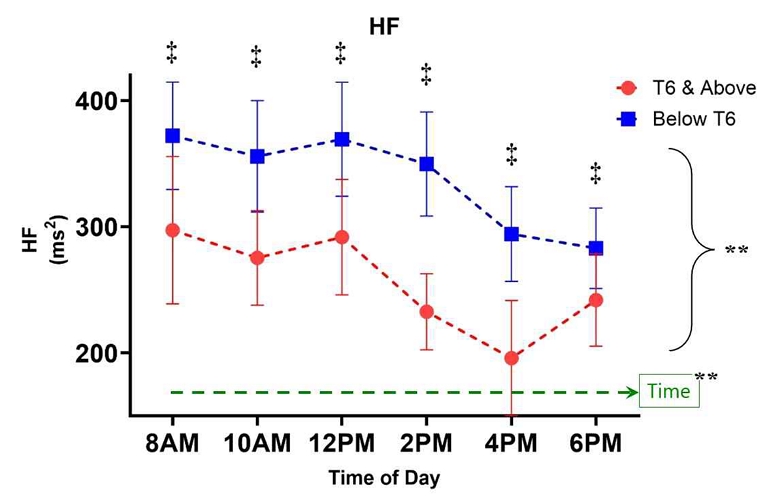
Power in high frequency(HF)
HF 지표의 경우, 구형성 가정이 충족되었고(Mauchly’s W=0.752, p=0.351), 시간에 따른 HF의 변화(주효과)는 통계적으로 유의하였다(F(5,57)=4.025, p=0.002, η²=0.067). 그룹 간 주효과는 유의하게 나타났고, T6 & Above 그룹과 Below T6 그룹 간의 평균에 유의한 차이가 있었다(F(1,56)=5.727, p=0.020, η²ₚ=0.093). 그룹과 시간의 상호작용 효과 또한 유의하여(F(5,57)=3.925, p=0.002, η²=0.065), 시간에 따른 HF 변화가 두 그룹 간에 다르게 나타남을 시사하였다. 반면, 시간과 성별, 연령 간의 상호작용 효과는 유의하지 않았다(p>0.05)(Figure 6). 사후분석 Shapiro-Wilk 검사 결과 대부분 시간대에서 정규성 가정 충족(p>0.05)하였고, 모든 시간대에서 Below T6 그룹이 T6 Above 이상 그룹보다 높은 HF 값을 보였으며, 특히 오후 시간대(2PM~6PM)에서 차이가 가장 두드러졌다(p<0.001). 대부분 시간대에서 d=0.57~0.86 수준으로 효과 크기(Cohen's d)는 중간이상 큰 크기이다.
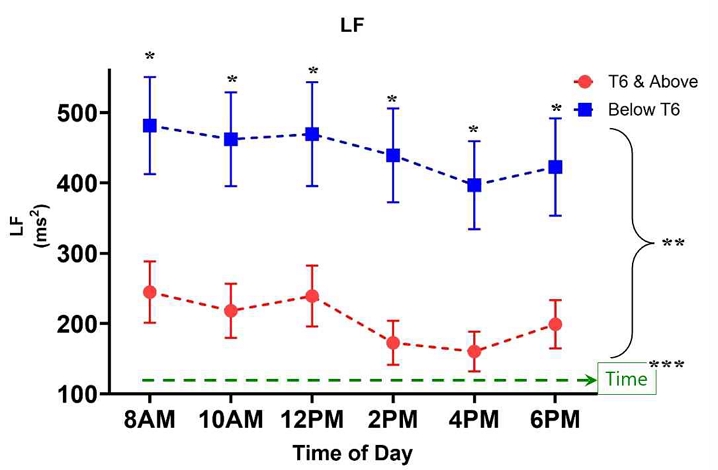
Power in lower frequency(LF)
LF 지표의 경우, 구형성 가정이 충족되었고(Mauchly’s W=0.776, p=0.473), 시간에 따른 LF의 변화(주효과)는 통계적으로 유의하였다(F(5,280)=5.494, p<0.001, η²=0.089). 또한 시간과 그룹 간의 상호작용 효과도 유의하게 나타났다(F(5,280)=2.842, p=0.016, η²=0.048). 정규성 검정(Shapiro-Wilk)은 대부분 시간대에서 정규성을 만족하였다(p>0.05). 효과크기(Cohen’s d=0.96~1.65)는 모든 시간대에서 0.96 이상으로, 그룹 간 큰 차이를 보였다. 사후검정 결과, 8AM 대비 2PM, 4PM, 6PM에서 LF 값이 유의하게 감소하였으며(p<0.001), 그룹 간에는 모든 시간대에서 Below T6 그룹이 T6 & Above 그룹보다 유의하게 높은 LF 값을 보였다(p<0.01). Levene’s Test에서 등분산성은 충족되지 않아, 각 시간대에서 그룹 간 비모수 검정(Mann-Whitney U test)을 시행하였고, 모든 시간대에서 유의한 차이(p<0.05)가 확인되었다(Figure 7).
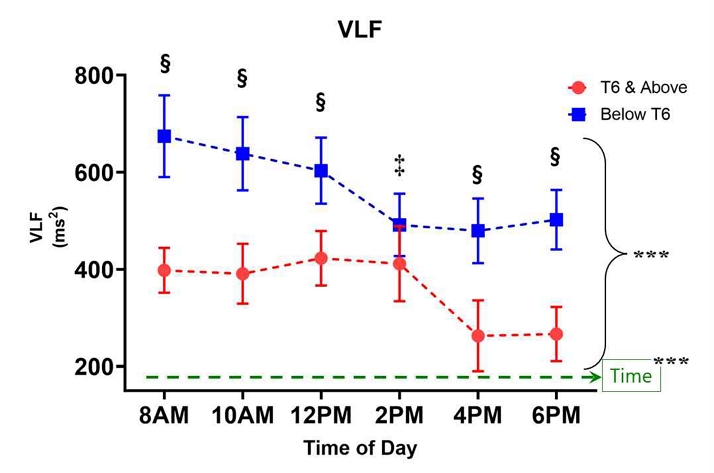
Power in Very lower frequency(VLF)
VLF 지표의 경우, 구형성 가정이 충족되지 않았다(Mauchly’s W=0.596, p=0.014). Greenhouse-Geisser 분석 결과, 시간에 따른 VLF의 변화(주효과)는 통계적으로 유의하였다(F(4.17, 233.27)=6.143, p<0.001, η²=0.099). 또한 시간과 그룹 간의 상호작용 효과도 유의하게 나타났다(F(4.17, 233.27)=11.812, p<0.001, η²=0.174). 그러나 시간과 성별 간(F=0.511, p=0.735), 시간과 연령 간(F=0.703, p=0.597)의 상호작용은 유의하지 않았다. 정규성 검정(Shapiro-Wilk)은 대부분 시간대에서 정규성을 만족하였다(p>0.05).
효과크기(Cohen’s d=0.96~1.65)는 모든 시간대에서 0.96 이상으로, 그룹 간 큰 수준으로 확인되었다. 사후 분석 결과, 그룹 간 2차(F=29.702, p<0.001), 4차(F=12.236, p<0.001), 5차(F=7.716, p=0.007)의 상호작용이 유의하여 시간에 따른 비선형적 차이가 나타났다. 단일 시간대 그룹 간 비교(Mann-Whitney U 및 t-검정)에서 T6 & Above 집단은 전반적으로 낮은 VLF 값을 보였으며, 모든 시간대에서 각 시간대별 그룹 간 유의한 차이를 보였다(p<0.01). 특히 8AM, 10AM, 12PM, 4PM, 6PM 시간대에서 두 집단 간 유의한 차이를 보였다(p<0.001). 효과크기(Cohen’s d)는 모든 시간대에서 큰 수준(0.82–1.67)으로 확인되었다. 대부분의 시간대에서 정규성을 만족하였으나(Shapiro-Wilk, p>0.05), 12PM 시간대의 T6 & Above 그룹은 p=0.041로 약간의 정규성 위배가 있어, 비모수 검정(Mann-Whitney U 및 t-검정)도 병행하였다(Figure 8).
LF/HF ratio
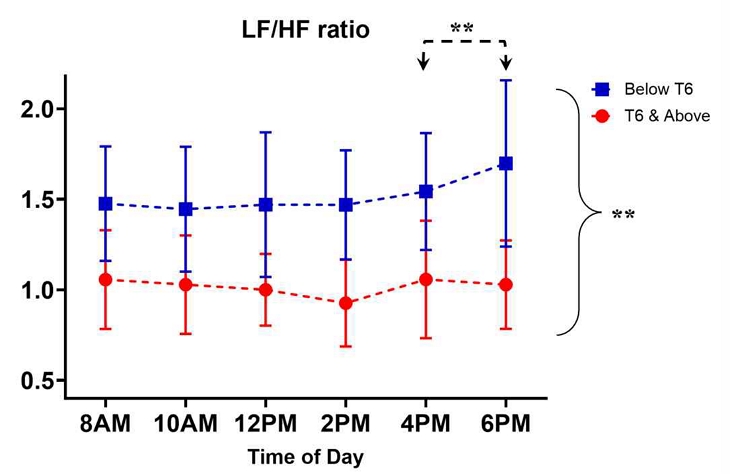
LF/HF 비율의 경우, 구형성 가정이 충족되었고(Mauchly’s W=0.783, p=0.507), 시간에 따른 LF의 변화(주효과)는 통계적으로 유의하지 않았다(F(5,280)=0.610, p<0.692, η²=0.011). 성별과 연령을 공변량으로 통제한 상태에서도 시간과 그룹 간의 상호작용 효과는 유의하지 않았다(F(5,280)=1.597, p=0.161, η²ₚ=0.028). 그룹간 주효과는 유의하였으며(F(1, 56)=126.406, p<0.001, η²=0.693), Low T6 그룹이 전반적으로 T6 & Above 그룹보다 높은 LF/HF 비율을 보였다. 다만 Bonferroni 방식으로 조정된 다중 대응비교 사후검정 결과, 4PM과 6PM 간의 LF/HF 비율 차이에서만 유의한 차이가 관찰되었다(p=0.016)(Figure 9).
Ⅳ. 고 찰
심박변이도 지표적 의미
본 연구는 급성 SCI 환자를 T6 척수신경을 기준으로 구분하여 낮 시간대, 즉 일상생활 중 자율신경계 기능을 HRV의 변화를 객관적으로 모니터링한 국내 최초의 연구이다. 주간 시간대의 HRV 그래프 분석시 자율신경계 기능의 시간적 역동성을 알 수 있었고, HRV 패턴 그래프는 이전 연구와 동일하였다(De Maria 등, 2023).
2008년 국내 성인을 대상으로 심박변이도를 하루 2회 오전, 오후의 변화를 관찰한 연구를 시작으로 2021년 정상 성인의 일 중 3회 측정한 연구(노은지 등, 2021)가 있었으나, 척수손상환자를 대상으로 한 국내 연구는 없으며, 최근 Saengsuwan 등이 보고한 SCI 환자의 HRV 24시간 변동 패턴과 비교해 보면, 낮 시간대의 변동 패턴과 상당수 일치한다(Saengsuwan 등, 2024). 해당 연구는 만성기 척수 손상환자를 모집하여 진행하였고, HRV는 늦은 오후에 가장 낮은 값을 보이고 이른 아침에 가장 높은 값을 보이는 패턴이 관찰되었다. Stampas 등의 연구에서는 급성 SCI 환자의 HRV를 입원 재활기간 동안 시간에 따라 분석하였고, 그 결과 패턴은 우리 연구의 결과와 일치한다 (Stampas 등, 2023). 또한 신경학적 회복이나 압력 손상과 같은 임상적 결과와의 연관성이 관찰되어, HRV가 자율신경계 기능 이상과 신경학적 회복의 임상적 결과에 영향을 줄 수 있음을 의미한다.
기존의 일중 연구는 대부분 만성 SCI 환자를 모집하여 안정적인 연구를 진행한 것에 비해, 본 연구에서는 초기입원 SCI 환자 118명 중 여러 사유로 58명이 누락되면서 6회 평가를 모두 완료한 환자는 약 50%인 60명이었다. 입원 중 안정적인 컨디션이 유지된 경우가 많아 기존 24시간 연구의 일중 HRV 리듬과 일치된 결과를 보였다(Besson 등, 2025; Hill 등, 2025; Saengsuwan 등, 2024; Vogiatzi 등, 2024; De Maria 등, 2023; Ruangsuphaphichat 등, 2023). 입원환자 중 불완전마비 환자의 경우에는 의학적 및 기능적 움직임에서 입원기간 중에 호전되는 양상으로 보여지고 있어, HRV에 대한 결과를 토대로 SCI의 예후와 연관성을 고려하는 연구가 필요할 수 있다.
교감신경-부교감신경 활동의 일주기 조절에 의한 HRV 일주기 리듬
자율신경계는 시상하부의 시교차상핵(SCN)에 위치한 생체 시계(circadian clock)에 의해 조절되며, 이는 혈압과 심박수의 일주기 리듬을 통해 HRV의 일중 변화를 유도한다. SCN은 심장과 혈관의 자율신경 활동을 매개하고, 이 과정에서 수면 상태와 체액성 매개체가 중요한 역할을 한다(Baschieri 등, 2019). 일반적으로 낮에는 교감신경 (SNS)이 우세하여 심박수가 증가하고 HRV가 감소하며, 밤에는 부교감신경(PNS)이 우세해져 HRV가 증가한다 (Baschieri 등, 2019; Crnko 등, 2019). 이러한 패턴은 HRV의 주파수 지표인 LF(교감 활성)와 HF(부교감 활성) 변화로 확인된다. Saengsuwan 등은 24시간 HRV 분석에서 낮 동안 LF 증가, 밤에는 HF 증가가 명확히 나타난다고 보고하였다(Saengsuwan 등, 2024). 이러한 리듬은 고혈압, 심부전, 당뇨병성 신경병증 등 다양한 질환의 자율신경 기능 평가에도 활용된다(Nagai 등, 2025; Karri 등, 2017; Graff 등, 2013). 또한, 코르티솔과 멜라토닌 같은 호르몬 분비도 일주기 리듬에 따라 조절되며, 아침에는 코르티솔 상승으로 HRV가 감소하고, 밤에는 멜라토닌 증가로 HRV가 증가한다(Morris 등, 2012).
생활습관 역시 HRV에 영향을 주며, 예를 들어 아침 운동은 HRV 증가에, 저녁 운동은 감소에 영향을 줄 수 있다(Frank 등, 2010). SNS와PNS의 균형은 정상 HRV 유지에 핵심적이며, 일주기 리듬을 고려하지 않은 HRV 해석은 한계가 있을 수 있다(Serhiyenko 등, 2025). 본 연구 결과에서도 오전 8시에 가장 HRV 파라미터 값들이 가장 크고, 낮에 감소하여 기존 연구와 일치하였고(Saengsuwan 등, 2024), Below T6 그룹의 RMSSD 값은 낮에 증가하는 양상은 이전 연구에서 정상인 그룹에서 보고된 그래프 양상에 가까이 다가갔다(Kim 등, 2021; Choi,등, 2020).
최근 스포츠 엘리트 선수들을 대상으로 집중적인 훈련의 전/후에 HRV를 측정하여 근력 및 지구력이 향상되는 교감신경의 영향을 분석하기 위한 연구에서 생리학적 지표로 활용되고 있으며, 운동 및 스포츠 의학 분야에서 일일(day-to-day) 측정값은 HRV가 훈련 부하, 회복 상태, 그리고 과훈련 위험을 측정하는 신뢰할 수 있는 지표 역할을 할 수 있음이 보고되었다(Iizuka 등, 2020; Lok 등, 2020). 이는 체계적인 HRV 평가에 따라 훈련 프로그램을 조정함으로써 부상이나 번아웃을 완화하는 동시에 신체의 컨디션을 신뢰할 수 있는 지표역할을 대표할 수 있음이 증명되었다(Besson, 등, 2025). SCI 환자에게 재활운동이 마비된 신체의 기능 회복에 효과적으로 적용되는 것을 모니터링하기 위해서는 운동 전/후 HRV의 변화를 관찰할 필요가 있으며(Kyriakides 등, 2019; Buker 등, 2018), 이를 위해서는 척수손상환자의 교감신경계 일주기 리듬을 고려한 측정이 필요하다(Saengsuwan 등, 2024). 엘리트 스포츠 선수들도 경기시간대에 맞춰서 신체 컨디션을 향상시키기 위해 일주기 리듬을 토대로 운동프로그램을 진행하듯이(Iizuka, 등, 2020; Lok 등, 2020), SCI 환자의 재활 훈련의 효과를 모니터링하기 위해서는 비슷한 시간대에서 측정한 HRV 결과값을 기준으로 재활치료 후 HRV 측정값을 비교하는 것이 바람직할 수 있다.
SCI 손상 레벨에 따른 HRV 변화
교감신경 분절은 주로 T1–T5 수준에서 심장에 분포하므로, T6 이상 손상 시 심장 교감신경 경로가 단절되어 자율신경 조절 기능이 현저히 저하된다(El-Kotob 등, 2018; Serra-Ano 등, 2015). 반면, T6 미만 손상에서는 심장 교감신경 전달 경로가 유지되므로 비교적 안정된 HRV 반응을 보이는 것으로 알려져 있다(Malmqvist 등, 2015; Serra-Ano 등, 2015). 이러한 해부학적 근거에 기반하여 T6를 기준으로 손상 수준을 상·하부로 나누어 심혈관계 자율신경 반응을 비교하는 접근이 널리 사용된다. 한편, 부교감신경(미주신경)은 뇌간에서 시작하므로 손상 수준에 관계없이 기능이 유지되는 반면(Seo 등, 2018; 김수진 등, 2014), T6 상위 손상에서는 교감신경계의 불활성과 부교감신경계의 상대적 우세로 인해 자율신경 균형의 붕괴가 나타나며, HRV 패턴에도 이에 따른 변화가 관찰된다(El-Kotob 등, 2018). 정상 성인의 경우에는 부교감신경 활성과 좌심실 충만도 간의 밀접한 연관성이 존재하지만, SCI 환자에서는 이러한 상관성이 소실된 것으로 보고된 바 있으며(Sharif 등, 2019; Biering-Sorensen 등, 2018; Karri 등, 2017), 이는 SCI에 의해 자율신경 기능과 심혈관 기능 간의 상호작용이 손상될 수 있음을 보고되었다.
SCI 환자는 건강한 성인에 비해 LF 파워, LF/HF 비율 값이 낮았고(Malmqvist 등, 2015), 본 연구에서도 기존 연구결과와 비슷한 값을 보였다. 본 연구에서도 T6 & Above 군에서는 SDNN, RMSSD, LF, HF의 유의한 감소가 관찰되었으며, 이는 이들 환자군에서 심혈관계의 자율신경 반응이 전반적으로 저하되어 있음을 보여준다. 특히 LF, HF의 동시 감소는 장기적인 심혈관 스트레스 상태 및 자율신경 기능 저하와 관련될 수 있으며, 이는 피로, 활력 감소, 정신적 부담감 등과 연관될 수 있다(Candia-Rivera 등, 2025; Serhiyenko 등, 2025; Yadav 등, 2025; van Es 등, 2024).
SDNN 값은 시간에 따른 변화는 크지 않으나, 손상 수준(T6 & Above vs. Below T6)에 따라 자율신경계 조절능력에서 뚜렷한 차이가 관찰되었다(p<0.001). 이전 결과에서 시간대별 변화보다는 손상수준에 따른 그룹 차이가 우세하므로, SCI 환자 임상연구에서 자율신경계 기능 평가 시에는 T6를 기준으로 그룹을 구분하는 것이 필요하다고 보고된 내용이 임상실험에서 중요함을 재확인하였다(Saengsuwan 등, 2024; Malmqvist 등, 2015).
RMSSD 값은 높을수록 부교감 신경의 조절이 우수함을 의미하는데, 일중 시간 경과에 따라 유의미하게 감소하여 발병초기 SCI 환자의 자율신경계 조절이 감소된 상태임을 확인하였다(Stampas, 등, 2023; Malmqvist 등, 2015). 오전보다 오후로 갈수록 더 RMSSD값이 감소함을 보였다. 정상인의 RMSSD 평균값은 약 20~40ms이나, 본 연구의 SCI 환자는 15~19ms로 평가되었고, 국내 성인을 대상으로 일중 2시간 간격으로 반복 검사를 시행한HRV 연구에서도 RMSSD 값은 오전보다 오후로 시간 흐름에 따라 감소하였는데(노은지 등, 2021), 척수손상환자를 평가한 본 연구에서도 오전 8시와 오후 6시 사이의 평균 RMSSD는 유의미하게 감소하였다(p<0.001). 하지만 척수신경 손상 수준의 영향은 다른 측정값에 비해 차이가 관찰되지 않았고, 성별, 나이와 시간 간의 상호작용 효과도 모두 통계적으로 유의하지 않았다. RMSSD 변화를 운동 강도 및 유형에 따라 운동 중과 운동 후 회복기에서 살펴보면, 운동 강도에 비례하여 유의하게 감소하였고, 중증도 이상의 강도에서는 RMSSD 감소 폭이 더 커졌는데, 이는 부교감신경이 억제되고 교감신경이 활성화되기 때문이다(최환석 등, 2005).
재활훈련프로그램에 의한 신체 움직임의 영향을 최소화하기위해 일요일에 측정하였고, 모든 척수손상환자의 이동을 보호자 혹은 평가자가 개인휠체어로 이동시키면서 대상자인 환자의 신체 움직임을 최소화한 것이 심장에 대한 스트레스 영향이 최소화되고, 심박수의 편차가 감소되어 손상수준에 따른 두 그룹 간의 RMSSD 차이가 적은 것으로 보인다. 또한 월요일부터 토요일까지 진행된 힘든 재활훈련 프로그램의 신체 피로가 누적되어 높은 스트레스 반응과 염증성 사이토카인 분비 증가로 인해 낮은 RMSSD값이 측정된 영향으로 볼 수도 있다(Kyriakides 등, 2019; Buker 등, 2018). 추후 유산소 운동과 근력운동의 전-후에 HRV 평가를 시행하여, 운동 종료 후 휴식 시간에 따라 RMSSD 감소된 값이 증가하는 것을 자율신경의 회복이 되는 지표(Orellana 등, 2019)로 모니터링하면 척수손상환자의 운동 후 부교감 신경계 활성화를 연구에 도움이 될 수 있다.
시간에 따른 HRV 변화
HF 파워는 Below T6 그룹이 T6 & Above 그룹에 비해 모든 시간대에서 일관되게 높은 값을 보였으며, 시간 경과에 따라 두 집단 모두에서 HF 파워가 점진적으로 감소하는 경향을 확인할 수 있었다. 특히, 집단에 따른 HF의 변화 곡선(이차 항) 역시 유의하게 달랐다(F=10.90, p=0.002). 집단별로 살펴보면, Below T6 그룹에서 모든 시간대에 걸쳐 T6 & Above 그룹보다 HF 값이 유의하게 높게 나타났고(예: 8AM 기준, Below T6 372.1±113.9 vs. T6 & Above 297.2±58.4 ms²). 시간대별로는 두 집단 모두 아침(8AM, 10AM, 12PM)에 비해 오후(2PM, 4PM)에서 HF 값이 감소하는 경향을 보였다. 이러한 HF 파워 결과는 SCI 환자에서 손상 레벨이 낮을수록, 즉 T6 이하일수록 높게 관찰되며, 시간 경과에 따른 감소 경향 역시 뚜렷하였다. 이는 최근 SCI HRV 연구 결과와 일치하며 (Hill 등, 2025; Calderon-Juarez 등, 2024; Park 등, 2024; Saengsuwan 등, 2024), 손상 수준에 따른 부교감 신경 활성도 차이, 즉 SCI 레벨이 낮을수록 부교감신경 활성(고주파 HRV, HF)이 더 잘 보존됨을 의미한다.
LF 파워는 T6 미만 손상 환자에서 유의하게 높게 유지되는 동시에(p=0.003), 시간 경과에 따라 감소하는 변화의 패턴은 두 그룹 모두에서 선형적 감소 양상이 뚜렷하게 나타났다(p=0.018). 이는 SCI에서 손상 수준이 자율신경계의LF 활성에 미치는 영향 및 일중 변화 양상에 대한 기존 연구 결과와 일치한다(Saengsuwan 등, 2024). 집단에 따른 LF의 변화 곡선(이차 항) 역시 유의하게 달랐다(F=10.90, p=0.002). 집단별로 살펴보면, Below T6 그룹이T6 & Above 그룹보다 모든 시간대에서 LF 값이 유의하게 높았다. 시간에 따른 LF 변화는 두 집단 모두에서 선형적 감소 경향 및 곡선(이차) 변화가 뚜렷하였다. 이러한 결과는 SCI 환자에서 손상 레벨에 따라 교감신경 활성(LF)의 절대치 및 변화 양상에 명확한 차이가 있음을 시사하며, 앉은 자세에서 HRV가 변경되어 있음을 발견하였다(Addleman 등, 2024; Calderon-Juarez 등, 2024; Park 등, 2024; Saengsuwan 등, 2024; Hodgkiss 등, 2023).
Below T6 그룹이 LF, VLF 모두에서 일관적으로 높았고, T6 & Above 그룹은 오후 4시에 가장 낮은 LF값을 보였다. LF와 VLF 모두 시간에 따라 유의하게 감소하면서, 오후/저녁으로 갈수록 큰 차이 발생하였다. VLF는 성별에 따라 유의한 차이 있으며(p=0.013), VLF 증가는 심혈관계 및 신경계 전반의 저활성 상태를 반영하는 지표로 해석될 수 있다.
T6 & Above 그룹과 Below T6 그룹 모두, 4PM와 6PM 시간대에서 HF, LF, VLF 파워값이 두드러진 감소 경향을 보였는데, 이는 초기 입원환자의 재활 훈련과정 중에 방광관리, 특히 넬라톤 등의 배뇨 훈련이 개인별 특정 시간대를 고려하여 진행되는 것과 관련이 있을 수 있다. 일반적으로 재원기간 중 방광관리를 함에 있어서 점심식사를 하고 나서 오후 4시경 방광에 소변이 충전되고, 배뇨 욕구를 느끼는 것과 배뇨 후에 방광이 비는 과정에서SDNN과 RMSSD의 감소가 관찰되었는데, 이는 최근 연구에서 SDNN과 RMSSD가 감소하였다는 보고와 일치하며, 가장 낮은 RMSSD와 SDNN 측정값은 심장의 변동이 최소인 시점으로, 방광이 가득차는 것으로 인한 스트레스 요인으로 인해 신체가 심한 부담을 받고 있음을 나타낸다(Calderon-Juarez 등, 2024). 이전 연구에서는 방광에 소변이 충전 단계에서 SDNN의 유의미한 변화가 보고되었고(p=0.042), 방광이 꽉 찰 때에 자율신경계 활동이 증가된 것이 HRV의 변화에 영향을 주는 것이 가능할 수 있음을 제안하였다. RMSSD가 감소했다가 크게 증가하는 이러한 패턴은 방광 충전 주기 동안 신체의 스트레스 반응과 이후 회복 단계 사이의 동적 변화를 의미한다 (Lee 등, 2017). Gomez 등의 연구에서는 배뇨에 대한 강한 욕구를 느낄 때, 정규화된 단위의 LF 평균은 증가, HF는 감소, LF/HF 비율은 증가한 연구를 보고하였고, 방광이 꽉 차면 교감신경이 우세한 방향으로 전환되었음을 보여주었다(Gomez 등, 2019). 이는 본 연구의 4PM에서 보여지는 HRV의 변화 패턴과 관련이 있을 수 있다. 또한 배뇨를 시도하여 방광이 비워진 후에는 LF/HF 비율은 1.2±0.6으로 감소하였고, LF는 44.1±14.5로 감소, HF는 41.2±13.2로 증가했으며, 이는 방광이 비워지면서 부교감신경이 활동적으로 진행된다는 것을 의미한다.
본 연구의 LF/HF 비율에 대한 일중 변화는 통계적으로 유의하지 않았으나, 그룹 간 주효과에서는 유의한 차이를 보였다. 특히 오후 6시에서 LF/HF 비율이 유의하게 증가한 점은 오후 4시에서 오후 6시 사이에서 T6 & Above 그룹은 LF/HF 비율에서 분자에 해당하는 LF 값은 두 그룹 모두 비슷한 비율로 증가한 반면, 분모에 해당하는 HF 값은 Below T6 그룹이 T6 & Above 그룹에 비해 상대적으로 증가하였다. 이는 기존의 연구(Krstacic 등, 2013; Jae 등, 2011)와 일치하며, 척수손상 환자의 자율신경 기능 모니터링에 있어 LF/HF 비율을 해석할 때에는 측정 시간대와 척수손상 수준을 모두 고려하는 것이 도움될 수 있다. T6 & Above 그룹의 환자들은 넬라톤 등을 통해 방광의 소변이 비워지면서 상대적으로 HF 값이 증가한 영향으로 보인다(Gomez 등, 2019; Mehnert 등, 2009). 또한 T6 & Above 그룹의 환자는 Below T6 그룹의 환자에 비해 교감신경 활성의 상대적 비중이 낮고, HF 값의 변화에 더 의존한다고 볼 수 있다. 즉 T6 & Above 그룹의 환자를 운동시킬 때, 오후 4시 이후에는 방광 배뇨 여부에 따른 영향을 고려하는 것이 필요할 수 있다. 즉 낮시간대에서도 오후 늦은 시간대에서 일중 변화에 영향을 주는 요인들이 존재할 가능성을 나타내며, 향후 보다 정밀한 반복 측정과 생체리듬 요소(예: 소변, 수면, 활동량) 통제가 필요한 것으로 사료된다. Krstacic 등은 급성 척수손상환자의 자율신경계 조절에 대한 연구를 하였고, 저주파 대 고주파 비율(LF/HF)이 경추 손상 그룹 40명(ratio 0.41)과 정상인 그룹 40명(ratio 1.71) 사이에서 통계적으로 유의미한 차이 있음을 보고하였다(Mann-Whitney U=0.0; Z=-7.7; p<0.001)(Krstacic 등, 2013). 본 연구의 LF/HF 비율 결과는 이전 연구의 경수손상 그룹(0.14)보다 본 연구의 T6 & Above 그룹 결과(1.02)가 크고, Below T6 그룹(1.52)은 이전 연구의 정상인 그룹(1.71)에 가까운 값을 보였다(Krstacic 등, 2013). 이런 LF/HF 비율 분석은 입원 초기 재활치료기간 동안 자율신경계 회복을 모니터링 함에 있어 도움될 수 있음을 보여주었다.
기존에 발표된 척수손상환자를 대상으로 HRV 양상을 연구한 대상자는 완전마비 비율이 높은 반면, 본 연구는 불완전 마비 중에서도 AIS-C & D 비율이 90%로 높아서 기존 연구의 결과들에 비해 조금씩 더 높은 결과값을 보였다(Yadav 등, 2025; Calderon-Juarez 등, 2024; Dorey 등, 2024; Hill 등, 2025; Park 등, 2024; Tsou 등, 2024; Saengsuwan, 등, 2024; Vogiatzi 등, 2024; Ruangsuphaphichat 등, 2023; Schoffl 등, 2023; Schoffl 등, 2023; Srirubkhwa 등, 2023; Stampas 등, 2023; Tsou 등, 2022).
초기 SCI 입원환자 대상 HRV 연구시 평가 시점의 중요성
SCI 환자에서 HRV의 임상적 활용에 있어 평가 시간대는 매우 중요한 변수이다. El-Kotob 등의 연구에서는 만성 외상성 SCI 환자(손상 후 평균 2년 이상)를 대상으로 LF와 HF 지표 간 높은 상관관계를 언급하였으나, 자율신경 균형을 의미하지는 않았고, 휴식 시 LF/HF 비율 단독 지표로는 해석에 한계가 있다는 점을 지적하였다(El-Kotob 등, 2018).
최근 Stampas 등의 연구에서는 입원 환자에게서 오전 7시와 오후 7시에 HRV를 각각 측정하여 일주기 내 변화를 비교하였으나, 전체 HRV 지표에서는 통계적으로 유의한 차이가 나타나지 않았고, 낮 시간대의 변화를 모니터링하지 못해 제한점을 남겼으나, 오후 세션에서 주파수 영역 지표의 변동성이 증가하는 경향을 보고하였고, 측정 시간의 일관성이 결과의 신뢰성을 높이는 요소로 작용할 수 있었다(Stampas 등, 2023). 이후 많은 연구에서 깨어 있는 낮 시간과 야간 수면 시간 간 HRV에 유의한 차이가 존재함을 보고되었고, 치료 반응 분석에서 측정 시간대를 설정하는 것이 중요한 변수가 될 수 있음을 제시하였다(Nagai 등, 2025; Park 등, 2024; Saengsuwan 등, 2024; Serhiyenko 등, 2025; van Es 등, 2024; Vogiatzi 등, 2024). 다른 연구에서는 입원 초기 사지마비 환자 24명을 대상으로 HRV 1회 측정하였고, AIS-A/B 수준에서 대부분의 환자가 평가되었고, 퇴원 시 AIS-C로 개선된 환자는 20.8%로 보고되었다(Nedumaran 등, 2022). 이는 초기 입원 환자 HRV 연구로서 의의는 있으나, 응급의료 및 수술 후 재활프로그램 등 의료시스템의 차이가 다를 수 있어, 신중한 접근이 필요하다.
Wecht 등의 연구에서는 침상에서 HRV 측정함으로 주위 환경의 자극을 최소화하였으나, 측정 시간대는 명확히 제시되지 않았다. 해당 연구에서는 NLI 또는 AIS 분류에 따라 평균 심박수나 혈압의 차이는 나타나지 않았지만, NLI 수준에 따라 HRV 지표와 미주신경 조절 간 선형적 연관성이 확인되었고, 손상 부위가 경수손상 수준으로 올라갈수록 HRV가 더 감소하는 경향이 있었다. 특히, AIS-A 환자는 기능이 일부 보존된 AIS-B~D 환자에 비해 교감신경의 혈관운동 조절 능력이 현저히 저하된 것으로 보고되었다(Wecht 등, 2022).
기존 임상 점수 체계(ISNCSCI 및 ISAFSCI)가 HRV나 메이어 파동(Mayer wave)과 같은 생리학적 지표와는 유의한 상관관계를 보이지 않는다는 보고가 있었고(Wecht 등, 2022), 자율신경계 기능의 평가에 있어 임상 점수만으로는 실제 기능 저하를 과소평가할 수 있다는 점이 제기되었다(El-Kotob 등, 2018). 또한, 신경병증 통증이 없는 SCI 환자에서는 건강한 대조군과 모든 시간 영역(SDNN, RMSSD) 및 주파수 영역(LF, HF, LF/HF) 분석에서, SCI 환자와 정상군 간 유의한 차이를 보이지 않았다는 연구들도 존재하며(Karri 등, 2017), 자율신경계 구조적 손상이 있더라도 신경병증 통증이 없는 경우에는 교감-부교감신경 균형이 보존될 수 있음을 제시하였으나, HRV 측정 시간대가 명확히 명시되지 않은 한계가 있다.
기존의 HRV 연구 대부분은 퇴원 후 안정된 SCI 환자를 대상으로 하였으며, 입원 초기 환자, 특히 낮 시간대에 반복 측정한 연구는 매우 드물다. 일부 연구에서 1회 측정으로 HRV를 분석하였으나(Stampas 등, 2023; Wecht, 등, 2022), 평가 시간이나 활동 상태에 대한 구체적 기술이 부족하여 해석에 제한이 있었다. 본 연구는 이와 달리 입원 초기 SCI 환자의 일상생활 환경 하에 2시간 간격으로 반복 측정한 자료를 제시함으로써, 보다 실제적인 자율신경 반응 변화를 확인하였다는 점에서 의의가 있다. HRV는 교감신경 및 부교감신경계의 기능을 반영하는 비침습적 지표로서, 자율신경계 평가 및 다양한 임상 조건에서의 예후 예측에 광범위하게 활용되고 있으나, HRV 지표를 단독 지표로 해석하기보다는 환자의 전반적인 임상 상태, 병력, 약물 복용 여부, 스트레스 수준 등을 함께 고려하여 다면적으로 해석해야 하며(De Maria 등, 2021; Guzzetti, 2001), 본 논문에서도 약물 복용시간 등이 결과값에 영양을 줄 수 있었지만, 입원환자의 특성상 약물복용 영향을 고려하거나, 통제할 수 없었다. 또한 HRV 값은 기록 시간(단기 vs. 장기), 분석 기법(FFT, AR 모델 등), 그리고 정규화(normalization) 방식에 따라 달라질 수 있으므로, 연구 간 비교 또는 환자 간 비교 시 주의가 필요하다(Candia-Rivera 등, 2025; Cowan, 1995).
호흡수, 혈압, 체온, 혈중 이산화탄소 농도 등 다양한 생리학적 인자가 HRV 매개변수, 특히 HF 파워(부교감신경 활성 반영)와 LF/HF 비율에 직접적인 영향을 미칠 수 있어서(Kuzmenko 등, 2022; Graff 등, 2013), 이런 외부 환경, 특히 적극적인 재활프로그램에 참여하면서 피곤하고 지치는 등(손경현 등, 2003; 윤홍일, 1997) 신체의 수많은 외부 자극 요인을 통제하기위해 일요일에 충분한 휴식을 취하면서 2시간 간격으로 평가하였다. 이에 시간에 따른 환자 개개인의 외부 변화를 통제하면서 측정할 수는 있었으나, 정확한 평가 시간대를 준수하면서 호흡수와 혈압, 체온 등의 모니터링까지 진행하기엔 제한적이었다. 특히 호흡 빈도의 증가나 얕은 호흡은 HF 파워를 과소평가하게 만들 수 있으며, 이는 교감-부교감 활동 균형의 왜곡된 해석으로 이어질 수 있고, 이러한 이유로 HRV는 자율신경계 기능을 정량화 하는 데 유용한 도구이지만, 해석할 때에는 반드시 측정 환경, 생리적 변수 및 개별 환자의 특성을 함께 고려하는 것이 필요하다. 단일 지표에 근거한 자율신경계 기능 판정은 제한적일 수 있다.
본 연구에는 몇 가지 제한점이 있다. 첫째, 사전 G*Power 분석에서 필요 표본 수를 76명으로 산출하였으나, 모집인원 118명에서 58명이 제외되면서 최종 분석에는 60명으로 진행되었다. 이러한 표본 수 부족은 특히 작은 효과 크기를 탐지하는 데 있어 통계적 검정력을 일부 감소시켰을 가능성이 있다. 따라서 통계적으로 유의하지 않은 결과 해석에는 주의가 필요하다. 둘째, HRV 측정은 단 하루에 한정되었기 때문에 개인 내 변화를 충분히 반영하지 못했을 수 있다. 셋째, 약물 복용이나 수면의 질과 같은 잠재적으로 영향받는 요인을 완전히 통제하지 못했다. 향후 연구에서는 더 큰 표본과 장기간의 모니터링을 통해 이러한 결과를 확증하고 확장할 필요가 있다. 이러한 제한점에도 불구하고 본 연구는 급성기 척수손상 환자가 손상 수준에 따라 뚜렷한 주간 HRV 양상을 보인다는 점을 새롭게 제시하였다. 이는 초기 재활 전략 수립과 임상적 자율신경 평가 개선에 중요한 기초 자료를 제공할 수 있다.
임상적 적용 가능성
본 연구는 임상적으로 중요한 의미를 제공한다. 급성기 SCI 환자의 자율신경계 기능은 손상 수준뿐 아니라 하루의 시간대에 따라서도 달라지므로, 임상 평가 시 두 요인을 함께 고려해야 한다. 실제로 발병 초기 입원한 척수손상 환자를 대상으로 낮 시간 동안 반복 측정한 HRV를 분석한 결과, 모든 시간대에서 T6 이하 손상군이 T6 이상 손상군보다 SDNN, RMSSD, HF, LF, VLF 값이 전반적으로 더 높았으며, 시간대에 따른 변화 폭 또한 더 크게 나타났다. 이러한 결과는 손상 수준에 따른 자율신경계 반응성 차이를 보여주는 생리적 지표로서, 향후 재활 중재 전후의 효과를 객관적으로 평가하는 데 활용될 수 있다. 낮 시간대 HRV 분석은 환자의 전반적인 신체 상태를 정밀하게 파악하고, 자율신경계 기능 저하에 따른 위험도를 사전에 분류하며, 이에 기반한 맞춤형 재활계획 수립 및 중재 반응 예측에 의미 있는 근거를 제공한다.
예를 들어, T6 이상 손상 환자의 경우 로봇보조보행치료를 오전 이른 시간, 오후 초반, 혹은 오후 늦은 시간에 시행할 때 자율신경계 반응과 신체 리듬이 달라질 수 있다. 이러한 이유로 인해 마비된 신체가 감당할 수 있는 운동량뿐 아니라 동일한 강도와 시간의 운동을 시행하였을 때, 그 효과에도 차이가 발생할 수도 있다. 이에 재활치료 효과를 극대화하기 위해서는 환자의 자율신경계 리듬과 일중 변화를 고려한 치료 일정 수립이 필요하다.
Ⅴ. 결 론
급성기 SCI 환자의 HRV는 하루 동안 시간대에 따라 유의하게 변하며, 손상 수준에 따라서도 자율신경계 반응에 차이가 존재함을 확인하였다. 특히 T6 이하 손상군은 SDNN, LF, HF, VLF 등 주요 지표에서 T6 이상 손상군보다 일관되게 높은 값을 보여 더 안정적인 자율신경 조절 기능을 시사하였다. 이러한 결과는 SCI 초기 단계에서 HRV를 통한 자율신경계 평가 시, 단일 시점 측정에 그치지 않고 시간대별 변화와 손상 수준을 함께 고려해야 함을 강조한다. 더 나아가 낮 시간대 HRV 모니터링은 환자의 자율신경 기능을 정밀하게 평가하고, 맞춤형 재활 전략 수립과 조기 치료 반응 예측에 활용될 수 있는 근거를 제공한다. RMSSD는 시간 경과에 따라 전반적으로 감소하는 경향을 보였으나, 손상 수준에 따른 상호작용은 확인되지 않았다. 또한 LF/HF 비율은 손상 수준에 따라 유의한 차이를 보이며, 자율신경계 균형에 대한 손상 수준의 영향을 나타내었다. 이러한 결과는 SCI 초기 단계에서 HRV를 통한 자율신경계 기능 평가 시, 단일 시점 외에 하루 시간대별 변화와 손상 수준을 함께 고려할 필요성을 제시하며, 맞춤형 재활 접근의 기초자료로 활용될 수 있다.
References
- 김수진, 고성은. 척수 손상 환자의 자율신경 반사이상 및 통증. 대한통증. 자율신경학회지. 2014;3(1):28–33.
- 김현철, 박기준. 국가대표 여자 유도선수들의 스포츠 손상과 심박변이도와의 스포츠 융합 분석. 한국융합학회논문지. 2020;11(4):49–54.
- 노은지, 최수지, 김덕호, 등. 건강인의 일중 심박변이도 변화 및 관련인자에 대한 예비연구. 대한한의학회지. 2021;42(2):50–61.
- 손경현, 김찬규, 방요순. 척수손상환자의 일상생활적응에 관한 연구. 대한물리치료과학회지. 2003:10(1):47-57.
- 신숙희, Shin SH. 생활 스트레스에 대한 심박변이와 혈청 코티졸과의 관계. 핵의학 기술. 2014;18(2):78–82.
- 윤홍일. 척수손상환자의 심리변화와 적응과정. 대한물리치료과학회지. 1997:4(4):529-538.
- 임창하, 우민정. 심박변이도 측정을 위한 디지털 기기의 활용은 적절한가? 심전도와의 비교를 통한 데이터 신뢰도 분석. 한국사회체육학회지. 2024;(98):325–36.
- 최환석, 옥선명, 김철민, 등. 유산소 운동이 Heart Rate Variability (HRV)에 미치는 영향. Korean J Fam Med. 2005;26(9):45–50.
-
Addleman JS, Lackey NS, DeBlauw JA, Hajduczok AG. Heart Rate Variability Applications in Strength and Conditioning: A Narrative Review. J Funct Morphol Kinesiol. 2024;9(2).
[https://doi.org/10.3390/jfmk9020093]

-
Baschieri F, Cortelli P. Circadian rhythms of cardiovascular autonomic function: Physiology and clinical implications in neurodegenerative diseases. Auton Neurosci. 2019;217:91–101.
[https://doi.org/10.1016/j.autneu.2019.01.009]

-
Besson C, Baggish AL, Monteventi P, et al. Assessing the clinical reliability of short-term heart rate variability: insights from controlled dual-environment and dual-position measurements. Sci Rep. 2025;15(1):5611.
[https://doi.org/10.1038/s41598-025-89892-3]

-
Biering-Sorensen F, Biering-Sorensen T, Liu N, et al. Alterations in cardiac autonomic control in spinal cord injury. Auton Neurosci. 2018;209:4–18.
[https://doi.org/10.1016/j.autneu.2017.02.004]

-
Buker DB, Oyarce CC, Plaza RS. Effects of Spinal Cord Injury in Heart Rate Variability After Acute and Chronic Exercise: A Systematic Review. Top Spinal Cord Inj Rehabil. 2018;24(2):167–76.
[https://doi.org/10.1310/sci17-00028]

-
Calderon-Juarez M, Miller T, Samejima S, et al. Heart Rate Variability-Based Prediction of Autonomic Dysreflexia After Spinal Cord Injury. J Neurotrauma. 2024;41(9-10):1172–80.
[https://doi.org/10.1089/neu.2023.0583]

-
Candia-Rivera D, de Vico Fallani F, Chavez M. Robust and time-resolved estimation of cardiac sympathetic and parasympathetic indices. R Soc Open Sci. 2025;12(1):240750.
[https://doi.org/10.1098/rsos.240750]

-
Choi J, Cha W, Park MG. Declining Trends of Heart Rate Variability According to Aging in Healthy Asian Adults. Front Aging Neurosci. 2020;12:610626.
[https://doi.org/10.3389/fnagi.2020.610626]

-
Chuangchai W, Pothisiri W. Postural Changes on Heart Rate Variability among Older Population: A Preliminary Study. Curr Gerontol Geriatr Res. 2021;2021:6611479.
[https://doi.org/10.1155/2021/6611479]

- Cohen J. Statistical Power Analysis for the Behavioral Sciences: L. Erlbaum Associates; 1988.
-
Cowan MJ. Measurement of heart rate variability. West J Nurs Res. 1995;17(1):32–48; discussion 101–11.
[https://doi.org/10.1177/019394599501700104]

-
Crnko S, Du Pre BC, Sluijter JPG, et al. Circadian rhythms and the molecular clock in cardiovascular biology and disease. Nat Rev Cardiol. 2019;16(7):437–47.
[https://doi.org/10.1038/s41569-019-0167-4]

-
de Carvalho Abreu EM, Dias LP, Lima FP, et al. Cardiovascular autonomic control in paraplegic and quadriplegic. Clin Auton Res. 2016;26(2):117–26.
[https://doi.org/10.1007/s10286-015-0339-1]

-
De Maria B, Dalla Vecchia LA, Porta A, et al. Autonomic dysfunction and heart rate variability with Holter monitoring: a diagnostic look at autonomic regulation. Herzschrittmacherther Elektrophysiol. 2021;32(3):315–9.
[https://doi.org/10.1007/s00399-021-00780-5]

-
De Maria B, Parati M, Dalla Vecchia LA, et al. Day and night heart rate variability using 24-h ECG recordings: a systematic review with meta-analysis using a gender lens. Clin Auton Res. 2023;33(6):821–41.
[https://doi.org/10.1007/s10286-023-00969-3]

-
Deshpande AK, Pande JA, Rohini A, et al. Heart Rate Variability: Objective Assessment of Autonomic Nervous System. MGM Journal of Medical Sciences. 2016;3(4):198–205.
[https://doi.org/10.5005/jp-journals-10036-1123]

-
Dorey TW, Nightingale TE, Alrashidi AA, et al. Effects of exercise on autonomic cardiovascular control in individuals with chronic, motor-complete spinal cord injury: an exploratory randomised clinical trial. Spinal Cord. 2024;62(10):597–604.
[https://doi.org/10.1038/s41393-024-01019-z]

-
El-Kotob R, Craven BC, Mathur S, et al. Assessing Heart Rate Variability As a Surrogate Measure of Cardiac Autonomic Function in Chronic Traumatic Spinal Cord Injury. Top Spinal Cord Inj Rehabil. 2018;24(1):28–36.
[https://doi.org/10.1310/sci17-00002]

-
Flueck JL, Schaufelberger F, Lienert M, et al. Acute Effects of Caffeine on Heart Rate Variability, Blood Pressure and Tidal Volume in Paraplegic and Tetraplegic Compared to Able-Bodied Individuals: A Randomized, Blinded Trial. PLoS One. 2016;11(10):e0165034.
[https://doi.org/10.1371/journal.pone.0165034]

-
Frank AJLS, Kun H, Heather E, et al. Impact of the human circadian system, exercise, and their interaction on cardiovascular function. Proc Natl Acad Sci U S A. 2010;107:20541–6 , publication_type = article.
[https://doi.org/10.1073/pnas.1006749107]

-
Gomez T, Gupta A, Rashmi Krishnan UK, et al. Correlation between Heart Rate Variability and Bladder Sensations During Filling and Voiding Phase of Urodynamic Study in Patients with Myelopathy. Ann Indian Acad Neurol. 2019;22(1):61–6.
[https://doi.org/10.4103/aian.AIAN_453_17]

-
Graff B, Gasecki D, Rojek A, et al. Heart rate variability and functional outcome in ischemic stroke: a multiparameter approach. J Hypertens. 2013;31(8):1629–36.
[https://doi.org/10.1097/HJH.0b013e328361e48b]

- Guzzetti S. Heart rate variability. Italian heart journal: official journal of the Italian Federation of Cardiology. 2001;2(5):450–4.
-
Henry M, Coxe RC, Barry A, et al. A research protocol to study the critical time window for rehabilitation after incomplete spinal cord injury: early vs. late locomotor training. BMC Neurol. 2024;24(1):482.
[https://doi.org/10.1186/s12883-024-03980-x]

-
Hill M, Jorgensen S, Engstrom G, et al. Cardiovascular autonomic function in middle-aged people with long-term cervical and upper thoracic spinal cord injuries. J Spinal Cord Med. 2025;48(3):447–60.
[https://doi.org/10.1080/10790268.2024.2403791]

-
Hodgkiss DD, Bhangu GS, Lunny C, et al. Exercise and aerobic capacity in individuals with spinal cord injury: A systematic review with meta-analysis and meta-regression. PLoS Med. 2023;20(11):e1004082.
[https://doi.org/10.1371/journal.pmed.1004082]

-
Iizuka T, Ohiwa N, Atomi T, et al. Morning Heart Rate Variability as an Indication of Fatigue Status in Badminton Players during a Training Camp. Sports (Basel). 2020;8(11).
[https://doi.org/10.3390/sports8110147]

-
Jae SY, Heffernan KS, Lee M, et al. Relation of heart rate recovery to heart rate variability in persons with paraplegia. Clin Auton Res. 2011;21(2):111–6.
[https://doi.org/10.1007/s10286-010-0096-0]

-
Kang H. Sample size determination and power analysis using the G*Power software. J Educ Eval Health Prof. 2021;18:17.
[https://doi.org/10.3352/jeehp.2021.18.17]

-
Karri J, Zhang L, Li S, et al. Heart Rate Variability: A Novel Modality for Diagnosing Neuropathic Pain after Spinal Cord Injury. Front Physiol. 2017;8:495.
[https://doi.org/10.3389/fphys.2017.00495]

-
Kim CW, Park KJ. Injuries and time loss in elite judo athletes: a Korean prospective cohort study. J Sports Med Phys Fitness. 2021;61(10):1380–6.
[https://doi.org/10.23736/S0022-4707.20.11760-2]

-
Kim HY. Statistical notes for clinical researchers: Sample size calculation 3. Comparison of several means using one-way ANOVA. Restor Dent Endod. 2016;41(3):231–4.
[https://doi.org/10.5395/rde.2016.41.3.231]

-
Kim SW, Park HY, Jung WS, et al. Predicting Heart Rate Variability Parameters in Healthy Korean Adults: A Preliminary Study. Inquiry. 2021;58:469580211056201.
[https://doi.org/10.1177/00469580211056201]

-
Kiyono K, Hayano J, Watanabe E, et al. Heart Rate Variability (HRV) and Sympathetic Nerve Activity. Clinical Assessment of the Autonomic Nervous System. 2017. p. 147–61.
[https://doi.org/10.1007/978-4-431-56012-8_9]

- Krstacic A, Krstacic G, Gamberger D. Control of heart rate by the autonomic nervous system in acute spinal cord injury. Acta Clin Croat. 2013;52(4):430–5.
-
Kuzmenko NV, Tsyrlin VA, Pliss MG. To the interpretation of frequency components of the heart rate variability. Translational Medicine. 2022;9(3):35–58.
[https://doi.org/10.18705/2311-4495-2022-9-3-35-58]

-
Kyriakides A, Poulikakos D, Galata A, et al. The effect of level of injury and physical activity on heart rate variability following spinal cord injury. J Spinal Cord Med. 2019;42(2):212–9.
[https://doi.org/10.1080/10790268.2017.1383709]

-
Lee ES, Joo MC. Prevalence of Autonomic Dysreflexia in Patients with Spinal Cord Injury above T6. Biomed Res Int. 2017;2017:2027594.
[https://doi.org/10.1155/2017/2027594]

-
Lok R, Zerbini G, Gordijn MCM, et al. Gold, silver or bronze: circadian variation strongly affects performance in Olympic athletes. Sci Rep. 2020;10(1):16088.
[https://doi.org/10.1038/s41598-020-72573-8]

-
Ma Y, Chang MC, Litrownik D, et al. Day-night patterns in heart rate variability and complexity: differences with age and cardiopulmonary disease. J Clin Sleep Med. 2023;19(5):873–82.
[https://doi.org/10.5664/jcsm.10434]

-
Malmqvist L, Biering-Sorensen T, Bartholdy K, et al. Assessment of autonomic function after acute spinal cord injury using heart rate variability analyses. Spinal Cord. 2015;53(1):54–8.
[https://doi.org/10.1038/sc.2014.195]

-
Mehnert U, Knapp PA, Mueller N, et al. Heart rate variability: an objective measure of autonomic activity and bladder sensations during urodynamics. Neurourol Urodyn. 2009;28(4):313–9.
[https://doi.org/10.1002/nau.20641]

-
Morris CJ, Yang JN, Scheer F. The impact of the circadian timing system on cardiovascular and metabolic function. Prog Brain Res. 2012;199:337–58.
[https://doi.org/10.1016/B978-0-444-59427-3.00019-8]

-
Myers J, Lee M, Kiratli J. Cardiovascular disease in spinal cord injury: an overview of prevalence, risk, evaluation, and management. Am J Phys Med Rehabil. 2007;86(2):142–52.
[https://doi.org/10.1097/PHM.0b013e31802f0247]

-
Nagai M, Ewbank H, Nakano Y, et al. Heart Rate Variability and Heart Failure with Reduced Ejection Fraction: A Systematic Review of Literature. Curr Cardiol Rev. 2025;21(2):78–87.
[https://doi.org/10.2174/011573403X327105241021180916]

-
Nedumaran L, Rebekah G, Tharion E, et al Initial Autonomic Parameters and Subsequent Short-Term Neurological Recovery after Inpatient Rehabilitation, in Traumatic Cervical Spinal Cord Injury Patients. Neurorehabil Neural Repair. 2022;36(4-5):269–73.
[https://doi.org/10.1177/15459683221081060]

-
Oka H. Heart Rate Variability and Neurological Disorders. Clinical Assessment of the Autonomic Nervous System. 2017. p. 179–97.
[https://doi.org/10.1007/978-4-431-56012-8_11]

-
Orellana JN, Nieto-Jiménez C, Ruso-Álvarez JF. Recovery slope of heart rate variability as an indicator of internal training load. Health. 2019;11(2):211–21.
[https://doi.org/10.4236/health.2019.112019]

-
Park HR, Ko HY, Kirshblum S, et al. Heart rate variability and its association with symptoms of orthostatic hypotension in spinal cord injury. J Spinal Cord Med. 2024:1–10.
[https://doi.org/10.1080/10790268.2024.2326703]

-
Park KJ, Jeong DN. Injuries pattern and heart rate variation in elite judo athletes: A Korean prospective cohort study. Sci Sports. 2022;37(5-6):496.e1–.e7.
[https://doi.org/10.1016/j.scispo.2022.03.001]

-
Rosado-Rivera D, Radulovic M, Handrakis JP, et al. Comparison of 24-hour cardiovascular and autonomic function in paraplegia, tetraplegia, and control groups: implications for cardiovascular risk. J Spinal Cord Med. 2011;34(4):395–403.
[https://doi.org/10.1179/2045772311Y.0000000019]

-
Ruangsuphaphichat A, Brockmann L, Sirasaporn P, et al. Test-retest reliability of short- and long-term heart rate variability in individuals with spinal cord injury. Spinal Cord. 2023;61(12):658–66.
[https://doi.org/10.1038/s41393-023-00935-w]

-
Saengsuwan J, Ruangsuphaphichat A, Brockmann L, et al. Diurnal variation of heart rate variability in individuals with spinal cord injury. Biomed Eng Online. 2024;23(1):58.
[https://doi.org/10.1186/s12938-024-01256-6]

-
Schoffl J, Arora M, Pozzato I, et al. Heart Rate Variability Biofeedback in Adults with a Spinal Cord Injury: A Laboratory Framework and Case Series. J Clin Med. 2023;12(24).
[https://doi.org/10.3390/jcm12247664]

-
Schoffl J, Craig A, McBain C, et al. The Effect of Non-Invasive, Non-Pharmacological Interventions on Autonomic Regulation of Cardiovascular Function in Adults with Spinal Cord Injury: A Systematic Review with Meta-Analysis. Neurotrauma Rep. 2024;5(1):1151–72.
[https://doi.org/10.1089/neur.2024.0110]

-
Schoffl J, Pozzato I, Rodrigues D, et al. Pulse rate variability: An alternative to heart rate variability in adults with spinal cord injury. Psychophysiology. 2023;60(11):e14356.
[https://doi.org/10.1111/psyp.14356]

-
Seo J-Y, Yoo J. Initial Assessment and Management of Patients with Spinal Cord Injury. Journal of Korean Society of Spine Surgery. 2018;25(2):81.
[https://doi.org/10.4184/jkss.2018.25.2.81]

-
Serhiyenko VA, Dolynay MI, Sehin VB, et al. Disorders of circadian rhythms of heart rate variability in diabetic cardiac autonomic neuropathy: mechanisms and consequences. INTERNATIONAL JOURNAL OF ENDOCRINOLOGY (Ukraine). 2025;20(8):549–58.
[https://doi.org/10.22141/2224-0721.20.8.2024.1461]

-
Serra-Ano P, Montesinos LL, Morales J, et al. Heart rate variability in individuals with thoracic spinal cord injury. Spinal Cord. 2015;53(1):59–63.
[https://doi.org/10.1038/sc.2014.207]

-
Sharif H, Wainman L, O'Leary D, et al. Cardiac parasympathetic activity and ventricular diastolic interactions in individuals with spinal cord injury. Spinal Cord. 2019;57(5):419–26.
[https://doi.org/10.1038/s41393-018-0224-6]

-
Solinsky R, Vivodtzev I, Hamner JW, et al. The effect of heart rate variability on blood pressure is augmented in spinal cord injury and is unaltered by exercise training. Clin Auton Res. 2021;31(2):293–301.
[https://doi.org/10.1007/s10286-020-00677-2]

-
Srirubkhwa S, Brockmann L, Vichiansiri R, et al. Reliability of five-minute vs. one-hour heart rate variability metrics in individuals with spinal cord injury. PeerJ. 2023;11:e16564.
[https://doi.org/10.7717/peerj.16564]

-
Stampas A, Malesovas C, Burke M, et al. Exploring 5-minute heart rate variability in spinal cord injury during acute inpatient rehabilitation. J Spinal Cord Med. 2023;46(3):450–7.
[https://doi.org/10.1080/10790268.2022.2052621]

-
Taralov ZZ, Terziyski KV, Kostianev SS. Heart Rate Variability as a Method for Assessment of the Autonomic Nervous System and the Adaptations to Different Physiological and Pathological Conditions. Folia Med (Plovdiv). 2015;57(3-4):173–80.
[https://doi.org/10.1515/folmed-2015-0036]

-
Tsou HK, Chen HY, Shih KC, et al. Para table tennis improves psychological/mental and cardiovascular health in individuals with spinal cord injury. NeuroRehabilitation. 2024;55(1):59–68.
[https://doi.org/10.3233/NRE-240083]

-
Tsou HK, Shih KC, Lin YC, et al. Altered heart rate variability and pulse-wave velocity after spinal cord injury. World J Clin Cases. 2022;10(27):9680–92.
[https://doi.org/10.12998/wjcc.v10.i27.9680]

-
van Es VAA, de Lathauwer ILJ, Kemps HMC, et al. Remote Monitoring of Sympathovagal Imbalance During Sleep and Its Implications in Cardiovascular Risk Assessment: A Systematic Review. Bioengineering (Basel). 2024;11(10).
[https://doi.org/10.3390/bioengineering11101045]

-
Vogiatzi G, Michou V, Malliaropoulos N, et al. Assessment of Cardiac Autonomic Function by Short-Term Sensor-Based and Long-Term Heart Rate Variability Analyses in Individuals with Spinal Cord Injury After Long-Term Table Tennis Training. Sensors (Basel). 2024;24(22).
[https://doi.org/10.3390/s24227167]

-
Wecht JM, Weir JP, Noonavath M, et al. Evaluation of Cardiovascular Autonomic Function during Inpatient Rehabilitation following Traumatic Spinal Cord Injury. J Neurotrauma. 2022;39(23-24):1636–44.
[https://doi.org/10.1089/neu.2021.0379]

-
West CR, Bellantoni A, Krassioukov AV. Cardiovascular function in individuals with incomplete spinal cord injury: a systematic review. Top Spinal Cord Inj Rehabil. 2013;19(4):267–78.
[https://doi.org/10.1310/sci1904-267]

-
Yadav RL, Martin JC, Galea MP. Evaluation and management of autonomic functions in patients with spinal cord injury: A scoping review. J Spinal Cord Med. 2025:1–61.
[https://doi.org/10.1080/10790268.2025.2485509]

-
Zimmermann G, Bolter LM, Sluka R, et al. Sample sizes and statistical methods in interventional studies on individuals with spinal cord injury: A systematic review. J Evid Based Med. 2019;12(3):200–8.
[https://doi.org/10.1111/jebm.12356]

-
Zhang H, Liu H, Gong M, et al. Analysis of changes in heart rate variability after prolonged ultra-high plateau residence in young healthy population: a cross-sectional study. Front Physiol. 2025;16:1529398:1-13
[https://doi.org/10.3389/fphys.2025.1529398]